Support hotline
400-810-0881
【ATCC新品】双荧光素报告癌症细胞系助力CAR-T细胞疗法
自2017年首个CAR-T疗法获批以来,目前已有多款CAR-T疗法获得FDA批准,主要用于治疗多种淋巴瘤、白血病和多发性骨髓瘤。然而,CAR-T疗法的研发远未止步——研究人员仍在探索新的靶点、优化CAR结构、拓展其在实体瘤中的应用,并尝试利用其他免疫细胞(如CAR-NK)构建新的治疗模式。
在这场持续进行的研发攻坚战中,一个关键问题始终困扰着科学家:我们如何真正“看见”CAR-T细胞在体内外的杀伤作用?
从“金标准”到“新视野”
传统的⁵¹Cr释放实验自1968年建立以来,一直是细胞毒性检测的“金标准”。它通过放射性铬标记靶细胞,检测细胞死亡后释放的放射性信号。但这种方法就只能证明CAR-T在培养皿里能杀死这些脑肿瘤细胞,却无法告知我们肿瘤细胞是如何形成又如何被杀死的。而且放射性物质的使用和处理让许多实验室望而却步,且会牺牲大量的实验动物。
单荧光素酶标记细胞的出现是一大进步,它让活体成像成为可能。但单荧光素酶系统就像一台只能告诉我们肿瘤细胞的荧光反应变弱了,却说不清是肿瘤细胞死了还是只是代谢活性下降。
如今,GFP与荧光素酶双报告细胞的出现,正在彻底改变这一局面。
ATCC的解决方案
为了更精准的判断CAR-T细胞的杀伤力,ATCC分别建了人源、鼠源个两种构同时稳定表达绿色荧光蛋白(GFP)和荧光素酶(Luc2)的双荧光素酶报告细胞:Raji-GFP-Luc2(ATCC® CCL-86-GFP-LUC2™)、NCI-H929-GFP-Luc2(ATCC® CRL-3580-GFP-LUC2™)和4T1-GFP-Luc2(ATCC® CCL-2539-GFP-LUC2™)、CT26.WT-GFP-Luc2(ATCC® CCL-26638-GFP-LUC2™)。
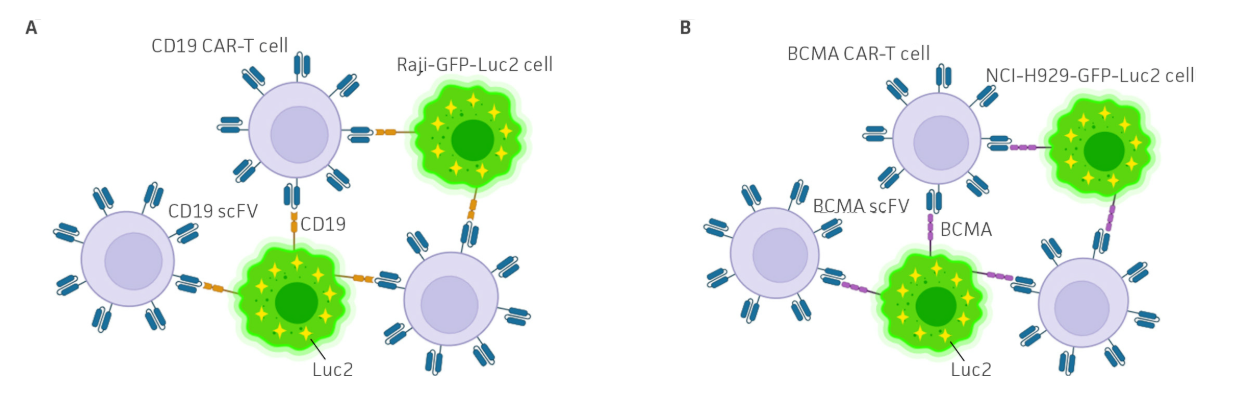
图1:CAR-T靶向双报告基因细胞。示意图展示(A)Raji-GFP-Luc2细胞(ATCC® CCL-86-GFP-LUC2™)和(B)NCI-H929-GFP-Luc2细胞(ATCC® CRL-3580-GFP-LUC2™)(绿色)在细胞表面表达CD19或BCMA的情况。抗原特异性CAR-T细胞(紫色)靶向报告细胞表面的CD19或BCMA。
由于荧光素酶表达与细胞数量相关,检测到的光强度降低意味着细胞数量减少,即细胞死亡增加。同样,通过荧光显微镜可实时监测表达荧光转基因的细胞,观察转基因表达的丧失情况。该方法能深入揭示CAR-T细胞靶向作用与杀伤癌细胞的动态过程。
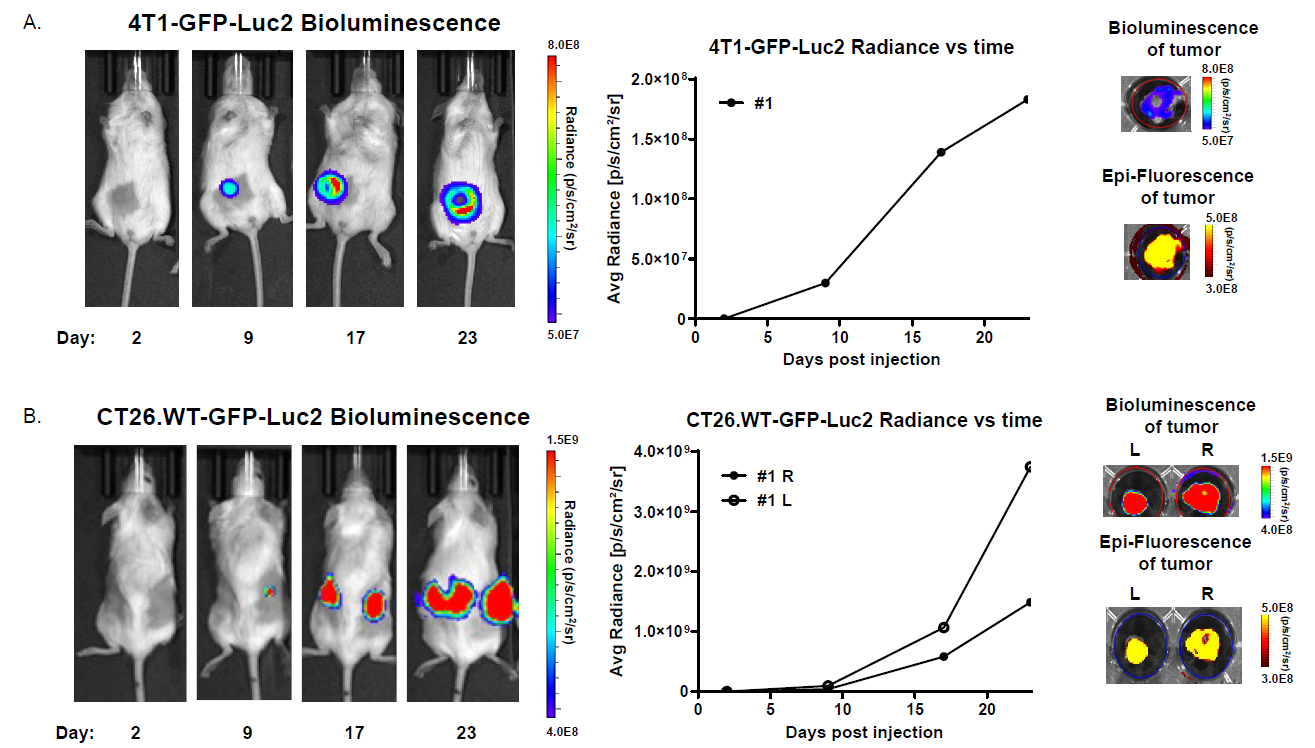
图2:4T1-GFP-Luc2与CT26.WT-GFP-Luc2细胞的体内荧光素酶活性检测。
ATCC双报告基因系统的优势
ATCC双报告基因细胞系是通过慢病毒转导技术,将 GFP-Luc2 双报告基因导入亲本肿瘤细胞系,经抗生素筛选、单细胞克隆后获得的稳定细胞株。这类细胞系既保留了亲本细胞的形态、生长动力学和致瘤性,又能稳定、高效表达 GFP 和荧光素酶,实现荧光成像和生物发光成像的双重检测。且两种信号强度均与细胞数量呈良好的线性相关,即使经过30次群体倍增,报告基因表达也不会显著下降。为各类体外、体内实验提供了稳定、可靠的检测基础。
相较于传统的⁵¹Cr释放实验,该双报告系统无需使用放射性同位素,操作流程更为安全简便。同时,它不仅能提供终点处的杀伤率,还能实现对整个杀伤过程的动态追踪。而相比于仅表达单一报告基因的细胞模型,双荧光素酶系统提供的双重信号可以相互印证。例如,当观察到活体成像信号下降时,结合体外GFP荧光强度的变化,有助于更全面地判断CAR-T细胞的效应,区分肿瘤细胞是被彻底清除还是仅进入低代谢状态。这种多参数的综合分析,为CAR-T细胞的功能研究、结构优化及联合治疗方案探索,提供了更为丰富和可靠的实验依据。
 京公网安备11010502040370号 Technical Support:Qingyun Software
京公网安备11010502040370号 Technical Support:Qingyun Software